Roxana Prudencio-Gamio
Silvia Echevarría-Lopez
Manuel Ccorahua-Paz
Carlos Ugas-Charcape
10.17843/rpmesp.2020.374.6198
ORIGINAL BREVE
Características clínicas y epidemiológicas de niños con COVID-19 en un hospital pediátrico del Perú
Clinical and epidemiological characteristics of children with COVID-19 in a pediatric hospital in Peru
Patricia Llaque-Quiroz ![]() 1,2, Médica/o cirujana/o; especialista en Neumología Pediátrica;
Magíster en Ciencias de Investigación Epidemiológica
1,2, Médica/o cirujana/o; especialista en Neumología Pediátrica;
Magíster en Ciencias de Investigación Epidemiológica
Roxana Prudencio-Gamio ![]() 1, Médica/o cirujana/o; especialista en Pediatría
1, Médica/o cirujana/o; especialista en Pediatría
Silvia Echevarría-Lopez ![]() 1, Médica/o cirujana/o; especialista en Neumología Pediátrica
1, Médica/o cirujana/o; especialista en Neumología Pediátrica
Manuel Ccorahua-Paz ![]() 1, Médica/o cirujana/o; especialista en Pediatría
1, Médica/o cirujana/o; especialista en Pediatría
Carlos Ugas-Charcape ![]() 1, Médica/o cirujana/o; especialista en Radiología
1, Médica/o cirujana/o; especialista en Radiología
1 Instituto
Nacional de Salud del Niño San Borja, Lima, Perú.
2 Universidad Peruana de Ciencias Aplicadas, Lima, Perú.
RESUMEN
Con el objetivo de conocer las características clínicas y epidemiológicas de niños con COVID‑19, se evaluaron las historias clínicas de pacientes atendidos de manera ambulatoria y en hospitalización del Instituto Nacional de Salud del Niño San Borja de marzo a mayo de 2020. Se registraron 33 pacientes, 57,6% fueron varones con mediana de edad de 4,8 años (rango: 2 meses - 17 años). El 81,8% tuvo contacto epidemiológico y la mediana del periodo de incubación fue siete días. El 60,6% tuvieron enfermedades concomitantes; el 93,9% presentó síntomas, los más comunes fueron fiebre y tos. El hemograma y los reactantes de fase aguda fueron normales en la mayoría de los casos. La radiografía de tórax fue anormal en 11/16 pacientes. El manejo fue de soporte, dos pacientes requirieron oxígeno suplementario. Un paciente falleció por complicaciones asociadas a una tumoración cerebral en fase terminal. Se reporta las caracteristicas clinicas y epidemiologicas en niños con COVID-19 durante los primeros meses de la pandemia en Perú.
Palabras clave: Nuevo Coronavirus 2019; Niños; SARS-CoV-2 (Fuente: DeCS BIREME).
ABSTRACT
The aim of the study was to describe the clinical and epidemiological characteristics of children with COVID-19. We analyzed the clinical records of inpatients and outpatients of the Instituto Nacional de Salud del Niño San Borja from the period between March and May, 2020. A total of 33 patients were registered, 57.6% were males with a median age of 4.8 years (range: 2 months - 17 years). We found that 81.8% of the children had contact with a positive COVID-19 case, 60.6% had concomitant diseases, 93.9% presented symptoms (mainly fever and cough) and the median incubation period was 7 days. The hemogram and acute-phase reactants were normal in most cases. Chest X-ray was abnormal in 11/16 patients. All patients received supportive treatment; 2 patients required supplemental oxygen. One patient died from complications associated with a terminal phase brain tumor. We report the clinical and epidemiological characteristics of children with COVID-19 during the first months of the pandemic in Peru.
Keywords: 2019 novel coronavirus; Children; SARS-CoV-2 (Source: MeSH NLM).
INTRODUCCIÓN
La infección por SARS-CoV-2 que causa la COVID-19 fue declarada pandemia el 11 de marzo de 2020. Se ha descrito que entre el 1 y el 6% de los casos corresponden a niños con una mortalidad menor que los adultos (1). En el Perú, se han reportado 683 687 casos de COVID-19 y 29 687 fallecidos, de los cuales 125 eran niños y adolescentes (2).
La COVID-19 en niños tiene características diferentes a la que presentan los adultos, como una mayor frecuencia de identificación del contacto intradomiciliario y la mayoría de pacientes son asintomáticos o tienen cuadros leves (3). Sin embargo, se ha reportado una presentación de inicio grave denominada síndrome inflamatorio multisistémico asociado al SARS-CoV-2, que se ha descrito solamente en niños (4).
Con respecto a los exámenes de laboratorio, se describen recuentos normales de leucocitos, linfocitos y neutrófilos en la mayoría de los casos. La elevación de reactantes de fase aguda no es frecuente en niños con COVID-19 (5). El engrosamiento peribronquial en la radiografía de tórax e imágenes en vidrio deslustrado en la tomografía de tórax son los hallazgos más frecuentes (6); sin embargo, son inespecíficos.
Las medidas que han mostrado utilidad en el manejo de los pacientes adultos con COVID-19 son el soporte ventilatorio y el uso de dexametasona en pacientes con insuficiencia respiratoria (7). No hay evidencia sobre la utilidad de otros tratamientos en niños.
En el Perú, no se disponen de reportes sobre las formas de presentación más comunes de COVID-19. Por ello, nuestro objetivo es describir las características clínicas y epidemiológicas de los niños atendidos en un hospital pediátrico de referencia nacional durante los primeros meses de la pandemia.
|
MENSAJES CLAVE |
|
Motivación para realizar el estudio: No se han reportado las formas de presentación más comunes de COVID-19 en niños en nuestro país. Principales hallazgos: Los síntomas iniciales de la COVID-19 en niños son similares a otros virus, con fiebre, síntomas respiratorios, digestivos y dérmicos. Estos síntomas son inespecíficos y el contacto epidemiológico es importante para el diagnóstico en niños. La evolución de los niños con comorbilidades fue favorable en la mayoría de los casos. Implicancias: La presentación de COVID-19 en niños es leve en la mayoría de casos, su tratamiento debe ser básicamente sintomático y de soporte. |
EL ESTUDIO
Se realizó un estudio descriptivo retrospectivo en pacientes menores de 18 años con diagnóstico de COVID-19 tratados de manera ambulatoria o en hospitalización del Instituto Nacional de Salud del Niño San Borja (INSNSB) durante el periodo marzo-mayo de 2020, se excluyeron los niños ingresados a cuidados intensivos. El muestreo fue no probabilístico por conveniencia con casos consecutivos.
Se revisó la historia clínica de los pacientes hospitalizados, las imágenes de tórax fueron evaluadas por un médico radiólogo pediatra. Se registraron los exámenes de laboratorio y las imágenes tomadas con la fecha más cercana a la fecha del inicio de los síntomas o del diagnóstico hasta un plazo de 72 horas antes o después de este.
El contacto con pacientes ambulatorios se realizó antes del estudio y como parte del monitoreo asistencial aprobado por la institución como una estrategia para detectar signos de alarma en pacientes con COVID-19 atendidos en el triaje diferenciado instalado desde el inicio de la pandemia. Se creó un sistema de seguimiento con un cuestionario estructurado como herramienta para registrar la información. El monitoreo consistió en una llamada telefónica con la identificación de datos epidemiológicos y signos de alarma, si estos últimos no estaban presentes, se brindaba educación sobre la prevención de contagios. Posteriormente, se hizo seguimiento telefónico cada 72 horas hasta la resolución de síntomas. Si se detectaban signos de alarma, se indicaba acudir a emergencia.
Se consideraron casos de COVID-19 a los niños con prueba de reacción en cadena de la polimerasa en tiempo real (RT-PCR, por sus siglas en inglés) para SARS-CoV-2 positiva o prueba serológica positiva (IgM e IgG, o IgM). El tipo de prueba serológica empleada fue cualitativa formato casete (Coretests®) y la muestra fue suero/plasma.
El análisis de datos se realizó con el paquete estadístico Stata versión 15.0. Las variables cualitativas se resumieron con frecuencias absolutas y relativas; las variables cuantitativas, con medidas de tendencia central y dispersión según normalidad.
Este estudio fue aprobado por el Comité de Ética del INSNSB (código PI-437). Solicitamos exención de consentimiento informado debido a que se trabajó exclusivamente con las historias clínicas y los registros médicos, no hubo contacto con los pacientes para fines del estudio. Los datos recolectados fueron resguardados en forma anónima y la base de datos se almacenará por tres años. Se asignó un código a cada paciente, sin que sea posible su identificación, lo cual aseguró la confidencialidad.
HALLAZGOS
Se evaluaron 33 niños con COVID-19, el 57,6% eran varones y la mediana de edad fue 4,8 años (rango: 2 meses - 17 años). El 63,6% (n = 21) de los pacientes fue tratado en hospitalización. El 60,6% de los pacientes tuvo comorbilidades, la mediana del número de comorbilidades fue 1 (rango: 0-5) y el tipo de comorbilidad más común fue la neurológica. De los niños seguidos de manera ambulatoria, solo tres tuvieron comorbilidades. El 81,8% de los pacientes tuvo contacto con una persona con COVID-19 y, la mayoría de las veces, el contacto fue intradomiciliario. La mediana del periodo de incubación fue siete días (rango intercuartil [RIC]: 4-15 días). El diagnóstico se hizo por resultado positivo de prueba molecular en 15/33 casos.
Del total de niños con COVID-19, 31/33 pacientes fueron sintomáticos. El 78,8% presentó fiebre, la mediana de los días de fiebre fue 2 (rango: 1-7) y el 57,6% tuvo tos. Otros síntomas menos frecuentes fueron los digestivos, los neurológicos y los dérmicos (Tabla 1). El 16,7% tuvo taquipnea, 23% taquicardia, la mediana de saturación fue 97% (RIC: 94-98%), y solo el 18,2% de los pacientes tuvo hallazgos anormales en el examen de tórax.
Tabla 1.Características clínicas y epidemiológicas de los niños con COVID-19 (n = 33).
|
Variables |
n (%) |
|
Sexo |
|
|
Masculino |
19 (57,6) |
|
Femenino |
14 (42,4) |
|
Edad en meses* |
58 (2-204) |
|
Lugar de tratamiento |
|
|
Hospitalario |
21 (63,6) |
|
Ambulatorio |
12 (36,4) |
|
Comorbilidades |
20 (60,6) |
|
Neurológica |
8 (40) |
|
Cardiopatía congénita |
4 (20) |
|
Digestiva |
2 (10) |
|
Otras |
6 (30) |
|
Antecedente de contacto COVID-19 |
|
|
Desconocido |
6 (18,2) |
|
Intradomiciliario |
13 (39,4) |
|
Extradomiciliario |
3 (9,1) |
|
Intrahospitalario |
11 (33,3) |
|
Periodo de incubación (días)** |
7 (4-15) |
|
Síntomas a la presentación |
|
|
Fiebre |
26 (78,8) |
|
Tos |
19 (57,6) |
|
Diarrea |
10 (30,3) |
|
Rinorrea |
9 (27,3) |
|
Náuseas o vómitos |
8 (24,2) |
|
Dolor faríngeo |
6 (21,2) |
|
Cefalea |
5 (15,2) |
|
Mialgias |
3 (9,1) |
|
Síntomas neurológicos |
3 (9,1) |
|
Lesiones dérmicas |
2 (6,1) |
*Mediana (rango)
**Mediana (rango intercuartil)
Los exámenes de laboratorio solo se realizaron en los pacientes hospitalizados, el hemograma y los reactantes de fase aguda fueron normales en la mayoría de pacientes (Tabla 2). 3 de 8 pacientes tuvieron resultados positivos de IgM frente a Mycoplasma pneumoniae, 1 de 13 tuvo hemocultivo positivo para S. aureus, 2 de 3 tuvieron resultados positivos del cultivo de secreciones respiratorias, uno a Stenotrophomona maltophila y uno a Pseudomona aeruginosa. El 60,7% de pacientes recibió antibióticos por coinfecciones.
Tabla 2.Resultados de los exámenes de laboratorio de niños hospitalizados con COVID-19 (n = 21)
|
Examen de laboratorio |
Resultados |
Valores normales |
|
Leucocitos (103/µL) |
8870 (6530-14 790) |
5-15,5 |
|
Neutrófilos (103/µL) |
4380 (2420-6652) |
1,5-8,5 |
|
Linfocitos (103/µL) |
2380 (1400-4040) |
2-8 |
|
Hemoglobina (g/dL) |
11,3 (10,4-12,7) |
11,5-13,5 |
|
Proteína C reactiva (mg/L) |
2,3 (0,75-26,65) |
<5 |
|
Procalcitonina (mg/dL) |
0,03 (0,02-0,13) |
<0,5 |
|
Deshidrogenasa láctica (U/L) |
650 (403-943) |
240-849 |
|
Ferritina (ng/mL) |
93 (55-1327) |
4-67 |
|
Dímero D (UEF/mL) |
0,58 (0,27-1,37) |
<0,5 |
|
CPK (U/L) |
55 (40-55) |
7-25 |
RIC: rango intercuartil, CPK: creatina fosfocinasa.
A 16 de 21 pacientes hospitalizados se les realizó radiografía de tórax. Se encontraron imágenes anormales en 68,8% (11/16). En los casos con imágenes anormales, lo más frecuente fue una afectación limitada, menor al 25% (63,6%, 7/11), de este grupo el hallazgo más frecuente fue engrosamiento peribronquial (Figura 1A). Solo tres pacientes tuvieron un compromiso extenso con consolidación y afectación mayor al 75% de ambos campos pulmonares (Figura 1B). A ningún paciente tratado de manera ambulatoria se le realizó radiografía de tórax.
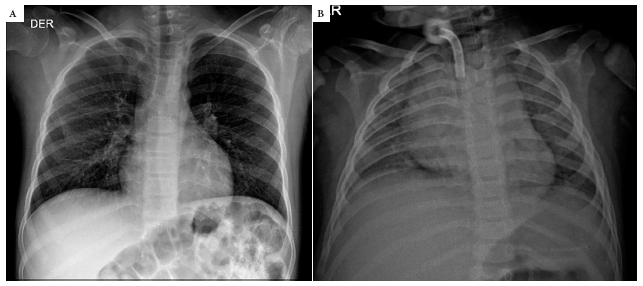
Figura 1. A. Niño de 12 años con antecedente de hemorragia intracerebral, padres con resultados de COVID-19 positivo. La radiografía simple de tórax muestra engrosamiento perihiliar bilateral. B. Niño de 2 años. La radiografía simple de tórax en anteroposterior muestra consolidación en ambos campos pulmonares con presencia de broncograma aéreo.
Todos los pacientes tratados de manera ambulatoria presentaron sintomatología leve y ninguno presentó complicaciones durante el seguimiento. Durante el estudio, ninguno de los pacientes hospitalizados ingresó a la unidad de cuidados intensivos a causa de la COVID-19. Un paciente falleció por complicaciones de hipertensión endocraneana por tumoración cerebral avanzada.
El tratamiento fue básicamente de soporte, en caso de fiebre o dolor, se usó paracetamol vía oral a dosis de 10 a 15 mg/kg hasta cada 4 horas. Un paciente recibió corticoides (dexametasona endovenosa, 0,3 mg/kg/dosis cada 12 horas) como parte del manejo de tumor intracraneal, y otro recibió enoxaparina subcutánea 1 mg/kg/dosis cada 12 horas durante su hospitalización por trombosis de vena cava secundaria a colocación de catéter venoso central. Los padres de dos pacientes atendidos por consulta ambulatoria les habían administrado ivermectina, pero no precisaron la dosis. Solo dos pacientes necesitaron oxígeno suplementario por cánula binasal.
DISCUSIÓN
Los casos de COVID-19 en niños, descritos en el presente estudio, corresponden a los primeros atendidos en un instituto de referencia nacional durante los primeros meses de la pandemia en el Perú. La mayoría de los pacientes eran de edad preescolar como se ha descrito en otras series (8); sin embargo, la infección puede presentarse en niños de todas las edades (9). El antecedente de contacto epidemiológico estuvo presente en el 82% de los casos y la mayoría de las veces dicho contacto fue intradomiciliario; se ha reportado información similar en otros estudios (10), y probablemente se deba a que, al suspenderse la educación presencial, los niños permanecen en el ambiente familiar durante la cuarentena obligatoria. La mediana del periodo de incubación ha sido de siete días, similar a lo reportado por Shen et al. (11).
Como lo reportado en otras series (12), la fiebre fue el síntoma más común en los niños, se presenta con valores menores a los 39 °C y dura menos de tres días, y la tos fue el segundo síntoma más frecuente. La cefalea y el dolor faríngeo fueron menos frecuentes que en adultos, debido a que estos síntomas no son expresados por niños pequeños. La presencia de taquipnea y hallazgos anormales en el examen de tórax fue infrecuente incluso en los pacientes hospitalizados y con hallazgos radiológicos anormales. Otros síntomas menos frecuentes fueron los gastrointestinales, con resultados similares a los reportados por Tian et al. (13), quienes encontraron que la diarrea es el síntoma gastrointestinal más común en niños, y que los vómitos se presentan con más frecuencia en niños que en adultos; estos hallazgos pueden deberse a la unión del SARS-CoV-2 a los receptores de la enzima convertidora de angiotensina 2 (ECA2) presentes en las células epiteliales esofágicas superiores y en las células epiteliales intestinales del íleon y el colon (14). Durante el periodo de evaluación, no hubo ningún caso de síndrome de respuesta inflamatoria multisistémica, que se ha reportado en etapas posteriores de la pandemia dado que en su origen pueden estar implicados mecanismos inmunológicos desencadenados por exposición previa al virus.
La mitad de los pacientes hospitalizados tenía comorbilidades complejas y en su mayoría fueron de carácter quirúrgico; sin embargo, ninguno de estos pacientes ingresó a cuidados intensivos como consecuencia de complicaciones propias de la infección. No hay evidencia suficiente sobre los factores asociados a complicaciones de COVID-19 en niños (15).
La mayoría de los pacientes evaluados presentó síntomas leves, como los descritos por Dong et al. (9), quienes reportaron que el 90% de niños diagnosticados con COVID-19 tenía enfermedad asintomática, leve o moderada. La menor susceptibilidad pediátrica a la infección por SARS-CoV-2 podría atribuirse a la menor expresión de los receptores celulares ECA2 y serina proteasa transmembrana 2 (TMPRSS2) en niños (14). Existen otras hipótesis como el entrenamiento de la inmunidad por el uso de vacunas vivas y la inmunidad cruzada con otras infecciones por coronavirus (16). Además, el menor daño endotelial en la edad pediátrica puede ser un factor protector, debido a que hay una relación directa entre daño endotelial y la respuesta inflamatoria al SARS-CoV-2 (14).
Los recuentos de series hematológicas estuvieron en su mayoría dentro de los límites normales y solo en dos niños se halló linfopenia. Se ha descrito que la mayoría de los niños presentan recuentos normales de leucocitos con hallazgo de neutrofilia y neutropenia en menos del 5% de los casos (5). La proteína C reactiva y la procalcitonina se encontraron elevados en el 13,6% y 10,6% de casos, respectivamente, porcentajes ligeramente mayores a los descritos por Wang et al. (12) que podría deberse a una coinfección bacteriana.
Para el estudio inicial de casos con presentación clínica moderada y grave, se sugiere la radiografía de tórax y se reserva la tomografía para casos con deterioro clínico (17). Las primeras series publicadas reportaron que la mayoría de los casos pediátricos tenían radiografías normales con escasos hallazgos (10,18). Sin embargo, en una serie en la que expertos en radiología pediátrica evaluaron 81 radiografías de niños con COVID-19, encontraron anormalidades en el 90% de los casos (6). En este estudio, se encontró que el porcentaje de pacientes con hallazgos anormales (63,8%) es mucho mayor a los reportes iniciales, esto podría deberse a que nuestra institución cuenta con un servicio de radiología dedicado a patología pediátrica; sin embargo, la proporción afectada fue menor a la serie presentada por Caro et al. (6)
Todos los niños con COVID-19 recibieron tratamiento sintomático y complementario cuando fue necesario. No se usó tratamiento farmacológico adicional al administrado para tratar el diagnóstico de fondo o una coinfección. Actualmente, no existe evidencia de tratamiento específico contra la COVID-19 y los ensayos clínicos aleatorizados con medicamentos han sido desarrollados en mayores de 12 años.
Solo un paciente murió por causas diferentes a la COVID-19 en el contexto de una enfermedad oncológica en cuidados paliativos. Se ha descrito que la mortalidad por COVID-19 en niños es menor que en adultos (19).
Al ser un estudio retrospectivo con revisión de historias clínicas, su principal limitación es la confiabilidad en el registro de la información. Además, su tamaño muestral es pequeño, debido a que se realizó en un solo centro y representa los primeros meses de la pandemia.
En conclusión, en esta serie, la presentación clínica de la COVID-19 en niños fue similar a otros virus, tuvo un curso leve en casi todos los casos y el antecedente epidemiológico fue importante para la sospecha diagnóstica.
Contribuciones de autoría: Todos los autores concibieron el estudio, diseñaron el trabajo de investigación, analizaron e interpretaron los datos, redactaron el artículo, aprobaron la versión final, y asumen la responsabilidad frente a todos los aspectos del manuscrito.
Conflictos de interés: Los autores no tienen ningún conflicto de interés que declarar.
Financiamiento: Autofinanciado.
REFERENCIAS BIBLIOGRÁFICAS
1. Wu Z, McGoogan JM. Characteristics of and Important Lessons from the Coronavirus Disease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72 314 Cases From the Chinese Center for Disease Control and Prevention. JAMA. 2020. doi: 10.1001/jama.2020.2648.
2. Ministerio de salud [Internet]. Lima: MINSA; 2020 [citado el 06 septiembre de 2020]. Disponible en: https://covid19.minsa.gob.pe/sala_situacional.asp.
3. Lu X, Zhang L, Li YY, Liu D, Shen K, Xu S, et al. SARS-CoV-2 Infection in Children. N Engl J Med. 2020;382(17):1663-5. doi: 10.1056/NEJMc2005073.
4. Verdoni L, Mazza A, Gervasoni A, Martelli L, Ruggeri M, Ciuffreda M, et al. An outbreak of severe Kawasaki-like disease at the Italian epicentre of the SARS-CoV-2 epidemic: an observational cohort study. Lancet. 2020;395(10239):1771-8. doi: 10.1016/S0140-6736(20)31103-X.
5. Henry BM, Lippi G, Plebani M. Laboratory abnormalities in children with novel coronavirus disease 2019. Clin Chem Lab Med. 2020;58(7):1135-8. doi: 10.1515/cclm-2020-0272.
6. Caro-Dominguez P, Shelmerdine SC, Toso S, Secinaro A, Toma P, Damasio MB, et al. Thoracic imaging of coronavirus disease 2019 (COVID-19) in children: a series of 91 cases. Pediatr Radiol. 2020;50(10):1354-68. doi: 10.1007/s00247-020-04747-5.
7. The RECOVERY Collaborative Group. Dexamethasone in hospitalized patients with Covid-19 -preliminary report. N Engl J Med. 2020. doi: 10.1056/NEJMoa2021436.
8. She J, Liu L, Liu W. COVID-19 epidemic: Disease characteristics in children. J Med Virol. 2020;92(7):747-54. doi: 10.1002/jmv.25807.
9. Dong Y, Mo X, Hu Y, Qi X, Jiang F, Jiang Z, et al. Epidemiology of COVID-19 Among Children in China. Pediatrics. 2020;145(6):e20200702. doi: 10.1542/peds.2020-0702.
10. Qiu H, Wu J, Hong L, Luo Y, Song Q, Chen D. Clinical and epidemiological features of 36 children with coronavirus disease 2019 (COVID-19) in Zhejiang, China: an observational cohort study. Lancet Infect Dis. 2020;20(6):689-96. doi: 10.1016/S1473-3099(20)30198-5.
11. Shen Q, Guo W, Guo T, Li J, He W, Ni S, et al. Novel coronavirus infection in children outside of Wuhan, China. Pediatr Pulmonol. 2020;55(6):1424-9. doi: 10.1002/ppul.24762.
12. Wang D, Ju XL, Xie F, Lu Y, Li FY, Huang HH, et al. Clinical analysis of 31 cases of 2019 novel coronavirus infection in children from six provinces (autonomous region) of northern China. Zhonghua Er Ke Za Zhi. 2020;58(4):269-74. doi: 10.3760/cma.j.cn112140-20200225-00138.
13. Tian Y, Rong L, Nian W, He Y. Review article: gastrointestinal features in COVID-19 and the possibility of faecal transmission. Aliment Pharmacol Ther. 2020;51(9):843-51. doi: 10.1111/apt.15731.
14. Yuki K, Fujiogi M, Koutsogiannaki S. COVID-19 pathophysiology: A review. Clin Immunol. 2020;215:108427. doi: 10.1016/j.clim.2020.108427.
15. Ludvigsson JF. Systematic review of COVID-19 in children shows milder cases and a better prognosis than adults. Acta Paediatr. 2020;109(6):1088-95. doi: 10.1111/apa.15270.
16. Dhochak N, Singhal T, Kabra SK, Lodha R. Pathophysiology of COVID-19: Why Children Fare Better than Adults?. Indian J Pediatr. 2020;87(7):537-46. doi: 10.1007/s12098-020-03322-y.
17. Foust AM, Phillips GS, Chu WC, Daltro P, Das KM, Garcia-Peña P, et al. International Expert Consensus Statement on Chest Imaging in Pediatric COVID-19 Patient Management: Imaging Findings, Imaging Study Reporting and Imaging Study Recommendations. Radiol Cardiothorac Imaging. 2020;2(2):e200214. doi: 10.1148/ryct.2020200214.
18. Cai J, Xu J, Lin D, Yang Z, Xu L, Qu Z, et al. A Case Series of children with 2019 novel coronavirus infection: clinical and epidemiological features. Clin Infect Dis. 2020:ciaa198. doi: 10.1093/cid/ciaa198.
19. Bai K, Liu W, Liu C, Fu Y, Hu J, Qin Y, et al. Clinical Analysis of 25 COVID-19 Infections in Children. Pediatr Infect Dis J. 2020;39(7):e100-3. doi: 10.1097/INF.0000000000002740.
Citar como: Llaque-Quiroz P, Prudencio-Gamio R, Echevarría-Lopez S, Ccorahua-Paz M, Ugas‑Charcape C. Características clínicas y epidemiológicas de niños con COVID-19 en un hospital pediátrico del Perú. Rev Peru Med Exp Salud Publica. 2020;37(4):689-93. doi: https://doi.org/10.17843/rpmesp.2020.374.6198.
Correspondencia: Patricia Beatriz Llaque Quiroz; Calle Santander 171, Dpto. 405, Miraflores. Lima, Perú; patriciallaque83@gmail.com
Recibido: 21/07/2020
Aprobado: 16/09/2020
En línea: 06/11/2020