Danitza Rojo García
Midori Torpoco Rivera
Paola Rondán-Guerrero
Frank García-Rojas
Alvaro Taype-Rondan
Original breve
Tendencias en el uso de fármacos para la COVID-19 durante la primera ola de la pandemia en un hospital de Lima, Perú
Trends in drugs usage for COVID-19 during the first wave of the pandemic in a hospital in Lima, Peru
Nataly Echevarria Castro ![]() 1
1
Danitza Rojo García ![]() 1
1
Midori Torpoco Rivera ![]() 1
1
Paola Rondán-Guerrero ![]() 1
1
Frank García-Rojas ![]() 2
2
Alvaro Taype-Rondan ![]() 3
3
1 Hospital Nacional Dos de Mayo, Lima, Perú
2 Sociedad Científica de San Fernando, Universidad Nacional Mayor de San Marcos, Lima, Perú
3 Universidad San Ignacio de Loyola, Unidad de Investigación para la Generación y Síntesis de Evidencias en Salud, Lima, Perú
Resumen
Con el objetivo de evaluar las tendencias en el uso de fármacos en pacientes con la COVID-19 de un hospital del Perú durante la primera ola de la pandemia se realizó un estudio retrospectivo entre abril y septiembre del 2020. Se revisaron las historias clínicas de pacientes hospitalizados por neumonía por COVID-19 en el Hospital Nacional Dos de Mayo (Lima, Perú). De un total de 3103 pacientes, se incluyeron 381 historias clínica (77,4% varones y mediana de edad de 44 años). Se observó un incremento del uso de cuatro fármacos prehospitalarios (azitromicina, ivermectina, corticoides y ceftriaxona), y una disminución del uso de seis fármacos intrahospitalarios (ceftriaxona, azitromicina, hidroxicloroquina, ivermectina, pulso de corticoides y anticoagulación profiláctica); además, el uso de anticoagulación intrahospitalaria aumentó. Estos hallazgos sugieren que el manejo de la COVID-19 varió durante la primera ola de la pandemia, aumentando el uso de fármacos prehospitalarios y disminuyendo el uso de fármacos intrahospitalarios.
Palabras clave: COVID-19; Neumonía; Terapéutica; Utilización de Medicamentos; Hospitalización; Factores epidemiológicos; Antibacterianos; Dexametasona; Perú; Tendencias (fuente: DeCS BIREME).
Abstract
This study aimed to evaluate the pharmacological trends in patients with COVID-19 from a hospital in Peru during the first wave of the pandemic. Retrospective study conducted between April and September 2020. The medical records of patients hospitalized for COVID-19 pneumonia at the Dos de Mayo National Hospital (Lima, Peru) were reviewed. Of a total of 3103 patients, 381 medical records were included (77.4% male, median age: 44 years). The use of four prehospital drugs increased (azithromycin, ivermectin, corticosteroids, and ceftriaxone), while the in-hospital use of six drugs (ceftriaxone, azithromycin, hydroxychloroquine, ivermectin, corticosteroid pulse, and prophylactic anticoagulation) decreased and in-hospital anticoagulation use decreased. These findings suggest that the management of COVID-19 has varied during the first wave of the pandemic, typically increasing prehospital drug use and decreasing inpatient use.
Keywords: COVID-19; Pneumonia; Therapeutics; Drugs Utilization; Hospitalization; Epidemiologic Factors; Anti-bacterial Agents; Dexamethasone; Peru; Trends (source: MeSH NLM).
INTRODUCCIÓN
En el mundo, el manejo farmacológico contra la COVID-19 se ha modificado con el pasar de los meses, predominando inicialmente un manejo empírico basado en la infodemia (1), que progresivamente fue dando lugar a un abordaje basado en evidencias (2). De esta manera, de los distintos fármacos que se han usado masivamente para el manejo de esta enfermedad (3–5), la mayoría finalmente dejaron de usarse por no mostrar beneficios (6).
En Perú, durante la primera ola de la COVID-19, el Ministerio de Salud (MINSA) estableció lineamientos para guiar su tratamiento. De manera que en abril del 2020 (7), estos lineamientos dieron potestad a los profesionales para usar azitromicina e hidroxicloroquina, como tratamiento específico en todos los casos; y antibioticoterapia y corticoterapia si hay evidencia de manifestación severa. En mayo, se agregó la ivermectina para casos leves, moderados y severos (8). En octubre, se modificaron las recomendaciones efectuadas (9), retirando la mayoría de los medicamentos ya expuestos y agregando el uso de anticoagulación profiláctica y corticoterapia en casos que requieran hospitalización.
En este contexto, el presente estudio tuvo por objetivo evaluar las tendencias en el uso de fármacos para la COVID-19 en pacientes hospitalizados durante la primera ola de la pandemia, en un hospital de Lima, Perú.
|
MENSAJES CLAVE |
|
Motivación: desde el inicio de la pandemia, el tratamiento de la COVID-19 se ha ido modificando; sin embargo, no se tiene conocimiento de las tendencias del uso de fármacos intra ni extrahospitalariamente. Principales hallazgos: encontramos un aumento en el uso de cuatro fármacos antes de la hospitalización (azitromicina, ivermectina, corticoides y ceftriaxona), y una disminución de uso seis fármacos (ceftriaxona, azitromicina, hidroxicloroquina, ivermectina, pulso de corticoides, y anticoagulación profiláctica) y el aumento en el uso de anticoagulación durante la hospitalización. Implicancias en salud publica: el conocimiento de las tendencias del uso de fármacos intra y extrahospitalariamente puede mejorar las decisiones de diversos sectores sanitarios en el Perú. |
EL ESTUDIO
Diseño y población
Estudio observacional retrospectivo analítico en pacientes adultos (≥ 18 años) del Hospital Nacional Dos de Mayo (Lima, Perú), hospitalizados entre el 1 de abril y el 30 de septiembre del 2020 con diagnóstico de neumonía por COVID-19 (CIE U07.1, U07.2). Estas fechas abarcan la primera ola de casos de COVID-19 en Perú.
Se incluyeron a pacientes con COVID-19 confirmado mediante una prueba molecular por reacción en cadena de la polimerasa con transcriptasa inversa y/o prueba rápida (IgM/IgG), así como aquellos con diagnóstico de caso probable de COVID-19 en base a criterios clínicos o imagenológicos. Se excluyeron gestantes, asintomáticos, y referidos de otro hospital.
Procedimientos
Durante enero del 2021, se solicitó al Hospital Nacional Dos de Mayo la lista de las historias clínicas de los pacientes hospitalizados por COVID-19 entre el 1 de abril y el 30 de septiembre del 2020. Esta lista incluyó 3103 historias, a las cuales se aplicó un muestreo aleatorio simple, calculando un tamaño de muestra para evaluar el uso de alguno de los medicamentos priorizados en el estudio. Para ello, se asumió de manera robusta una proporción esperada del 50%, y un nivel de confianza del 95%, obteniendo un tamaño de muestra mínimo de 342, al cual se agregó aproximadamente un 10% para amortiguar pérdidas, obteniendo finalmente 388 historias.
Se elaboró una ficha electrónica ad-hoc en Microsoft Excel. Se solicitó acceso a las historias clínicas aleatorizadas al Departamento de Archivos e Historias Clínicas, y tres investigadores (DRG, NEC y MTR) tuvieron el acceso a las historias (que se encuentran solamente en formato físico), verificaron que cumplan con los criterios de inclusión, y recolectaron las variables de interés consignadas en la ficha electrónica. Posteriormente, otro investigador (NEC) volvió a revisar todos los datos de interés para confirmar que la digitación haya sido correcta.
Variables
La variable independiente fue la fecha de ingreso a hospitalización. Las variables dependientes fueron el uso de medicamentos antes y durante la hospitalización.
Sobre el uso de fármacos prehospitalarios: al ingreso del paciente al hospital, los médicos tratantes indagaron (mediante anamnesis directa o indirecta) si el paciente había usado estos medicamentos para el tratamiento de la COVID-19 previo a la hospitalización: azitromicina, ivermectina, corticoides, ceftriaxona, anticoagulantes, e hidroxicloroquina. En cada caso, la variable fue recolectada de forma dicotómica (usó ese fármaco prehospitalariamente o no).
Sobre el uso de fármacos intrahospitalarios: durante la hospitalización se registraron en las historias clínicas los medicamentos que se brindaron a los pacientes. Se evaluaron los siguientes medicamentos: corticoides (a dosis usual y en pulsos), anticoagulación (plena y profiláctica), ceftriaxona, azitromicina, hidroxicloroquina, ivermectina, y tocilizumab. En cada caso, la variable fue recolectada de forma dicotómica (usó ese fármaco durante la hospitalización o no).
Otras variables recolectadas fueron edad, sexo, lugar de procedencia, saturación de oxígeno (SatO2) al ingreso, fracción inspirada de oxígeno (FiO2), SatO2/FiO2, y el tiempo desde el inicio de síntomas hasta la hospitalización.
Análisis estadístico
La base de datos fue exportada para el análisis al programa estadístico Stata v14.0 (Statacorp, TX, USA). Para el análisis univariado se calcularon proporciones, medidas de tendencia central y de dispersión. Se elaboraron gráficos de líneas para mostrar las tendencias.
El mes de ingreso se dividió en tres categorías (abril a mayo, junio a julio, y agosto a septiembre), intentando que el número de observaciones sea balanceado entre los grupos para permitir una comparación adecuada. Se evaluó la asociación entre esta variable y la frecuencia de uso de cada fármaco; siempre que el fármaco tuviera una frecuencia de uso entre 10% y 90%, para permitir el modelamiento estadístico. Para ello, se calcularon razones de prevalencias crudas (RP) y ajustadas (RPa), con sus intervalos de confianza al 95% (IC 95%) usando regresiones de Poisson con varianza robusta. Se consideró como potenciales confusores el sexo, la edad (en terciles), la SatO2/FiO2 (en terciles), y el tiempo desde el inicio de síntomas hasta la hospitalización (en terciles).
Criterios éticos
El estudio fue aprobado por el comité de Ética del Hospital Nacional Dos de Mayo (0234-2021-OACDI-HNDM).
HALLAZGOS
Se revisaron 388 historias clínicas de pacientes adultos hospitalizados por COVID-19 registrados en el Hospital Nacional Dos de mayo, de las cuales se excluyeron siete por ser pacientes referidos de otro hospital, incluyendo finalmente 381 historias clínicas. De estos, 77,4% fueron de sexo masculino, la mediana de edad fue 44 años, el 97,1% provenían de Lima Metropolitana y el 11,4% estaban con oxígeno suplementario al ingreso (Tabla 1).
Tabla 1. Características de los pacientes incluidos en el estudio, al momento del ingreso (n=381).
|
Característica |
n (%) |
|
Mes de ingreso |
|
|
Abril |
45 (11,8) |
|
Mayo |
35 (9,2) |
|
Junio |
85 (22,3) |
|
Julio |
103 (27,0) |
|
Agosto |
79 (20,7) |
|
Setiembre |
34 (8,9) |
|
Edad en años, mediana (rango intercuartílico) |
44 (55 - 65) |
|
Sexo masculino |
295 (77,4) |
|
FiO2 |
|
|
Oxígeno suplementario |
43 (11,4) |
|
FiO2 ambiental <85% |
121 (36,1) |
|
FiO2 ambiental entre 85 a 90% |
130 (38,8) |
|
FiO2 ambiental >90% |
84 (25,1) |
|
índice SatO2/FiO2 (en terciles) |
|
|
22 a 380 |
131 (34,8) |
|
381 a 425 |
130 (34,5) |
|
426 a 471 |
116 (30,8) |
|
Tiempo desde inicio de síntomas hasta la hospitalización |
|
|
0 a 7 días |
187 (49,1) |
|
8 a 11 días |
89 (23,4) |
|
12 a más días |
105 (27,6) |
|
Uso de fármacos antes del ingreso |
|
|
Algún fármaco |
166 (44,0) |
|
Azitromicina |
121 (32,0) |
|
Ivermectina |
110 (28,9) |
|
Corticoides |
79 (20,7) |
|
Ceftriaxona |
52 (13,7) |
|
Anticoagulantes |
19 (5,0) |
|
Hidroxicloroquina |
5 (1,3) |
|
Uso de fármacos durante la hospitalización |
|
|
Algún fármaco |
362 (99,7) |
|
Corticoides |
330 (88,2) |
|
Anticoagulación plena |
319 (84,8) |
|
Ceftriaxona |
274 (73,3) |
|
Azitromicina |
174 (46,4) |
|
Hidroxicloroquina |
95 (25,4) |
|
Ivermectina |
83 (22,1) |
|
Pulsos de corticoides |
81 (21,5) |
|
Anticoagulación profiláctica |
66 (17,7) |
|
Tocilizumab |
48 (12,9) |
SatO2: saturación de oxígeno, FiO2: fracción inspirada de oxígeno
Con respecto al uso de fármacos antes del ingreso al hospital, el 44,0% de los pacientes usaron algún fármaco: 32,0% azitromicina, 28,9% ivermectina, 20,7% corticoides, 13,6% ceftriaxona, 5,0% anticoagulantes y 1,3% hidroxicloroquina (Tabla 1). Las regresiones ajustadas (Tabla 2) y el gráfico (Figura 1A) muestran que la frecuencia de consumo de algún fármaco aumentó a lo largo de los meses. Este aumento fue temprano (logrando mesetas desde junio) para azitromicina, ivermectina, y corticoides; y fue tardío (alcanzando el pico recién entre agosto y septiembre) para ceftriaxona. No se pudo evaluar diferencias en el uso de anticoagulantes ni hidroxicloroquina debido a su baja frecuencia.
Tabla 2. Factores asociados al uso de fármacos antes de la hospitalización.
|
Fármacos |
n (%) |
RP
crudo |
RP
ajustado b |
|
Algún fármaco previo a |
|
|
|
|
Abril a mayo |
13 (16,3) |
Ref |
Ref |
|
Junio a julio |
94 (50,0) |
3,08 (1,83 - 5,17) |
3,25 (1,88 - 5,62) |
|
Agosto a setiembre |
61 (54,0) |
3,32 (1,96 - 5,62) |
3,39 (1,96 - 5,87) |
|
Azitromicina |
|
|
|
|
Abril a mayo |
8 (10,0) |
Ref |
Ref |
|
Junio a julio |
73 (39,2) |
3.92 (1,98 - 7,76) |
4,40 (2,12 - 9,14) |
|
Agosto a setiembre |
40 (35,7) |
3,57 (1,77 - 7,22) |
3,84 (1,82 - 8,10) |
|
Ivermectina |
|
|
|
|
Abril a mayo |
8 (10,0) |
Ref |
Ref |
|
Junio a julio |
65 (34,6) |
3,46 (1,74 - 6,87) |
3,44 (1,71 - 6,91) |
|
Agosto a setiembre |
37 (32,7) |
3,27 (1,61 - 6,66) |
3,20 (1,58 - 6,49) |
|
Corticoides |
|
|
|
|
Abril a mayo |
5 (6,3) |
Ref |
Ref |
|
Junio a julio |
45 (23,9) |
3,83 (1,58 - 9,30) |
3,67 (1,50 - 8,94) |
|
Agosto a setiembre |
29 (25,7) |
4,11 (1,66 - 10,16) |
3,57 (1,46 - 8,74) |
|
Ceftriaxona |
|
|
|
|
Abril a mayo |
4 (5,0) |
Ref |
Ref |
|
Junio a julio |
20 (10,6) |
2,13 (0,75 - 6,03) |
2,02 (0,69 - 5,91) |
|
Agosto a setiembre |
28 (24.8) |
4,96 (1,81 - 13,59) |
4,78 (1,76 - 12,97) |
a Algún fármaco previo: azitromicina, ivermectina, corticoides, ceftriaxona, anticoagulación, hidroxicloroquina, dióxido de cloro.
b RP ajustado por sexo, edad (en terciles), SatO2/FiO2 (en terciles), y tiempo desde
el inicio de síntomas hasta la hospitalización (en terciles).
RP: razones de prevalencia, IC 95%: intervalo de confianza al 95%.
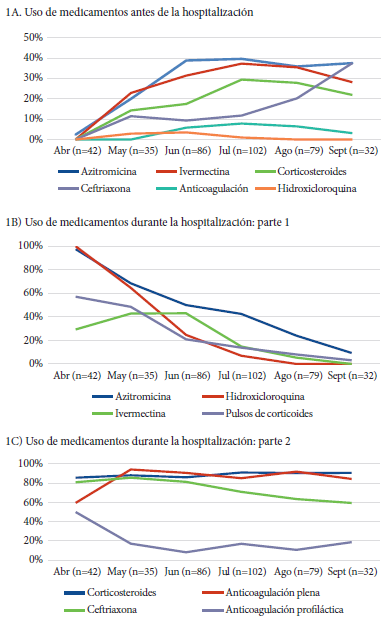
Figura 1. Tendencias en el uso de medicamentos antes de llegar al hospital, y durante la hospitalizacion.
Con respecto al uso de fármacos durante la hospitalización, a 99,7% de los pacientes se les brindó alguno de los fármacos evaluados: 88,2% corticoides, 84,8% anticoagulación plena, 73,3% ceftriaxona, 46,4% azitromicina, 25,4% hidroxicloroquina, 22,1% ivermectina, 21,5% pulsos de corticoides, 17,7% anticoagulación profiláctica, y 12,9% tocilizumab. Las regresiones ajustadas (Tabla 3) y las gráficas (Figuras 1B y 1C) muestran una disminución estadísticamente significativa en la frecuencia de uso de seis tratamientos. Esta disminución ocurrió tempranamente (en junio) para azitromicina, hidroxicloroquina, pulsos de corticoides, y anticoagulación profiláctica; y tardía (en agosto) para ceftriaxona e ivermectina. Asimismo, se encontró un incremento temprano en la frecuencia de uso de anticoagulación plena y no se evidenciaron cambios significativos en dos tratamientos (corticoides a dosis estándar y tocilizumab).
Tabla 3. Factores asociados al uso de fármacos durante la hospitalización.
|
Fármacos |
n (%) |
RP crudo (IC 95%) |
RP ajustado a (IC 95%) |
|
Corticoides |
|
|
|
|
Abril a mayo |
67 (84,8) |
Ref |
Ref |
|
Junio a julio |
166 (88,8) |
1,05 (0,94 - 1,16) |
1,06 (0,95 - 1,18) |
|
Agosto a setiembre |
97 (89,8) |
1,06 (0,95 - 1,19) |
1,04 (0,93 - 1,17) |
|
Anticoagulación plena |
|
|
|
|
Abril a mayo |
59 (73,8) |
Ref |
Ref |
|
Junio a julio |
164 (87,7) |
1,19 (1,03 - 1,37) |
1,21 (1,05 - 1,40) |
|
Agosto a setiembre |
96 (88,1) |
1,19 (1,03 - 1,38) |
1,20 (1,03 - 1,39) |
|
Ceftriaxona |
|
|
|
|
Abril a mayo |
66 (82,5) |
Ref |
Ref |
|
Junio a julio |
141 (75,8) |
0,92 (0,81 - 1,05) |
0,91 (0,80 - 1,04) |
|
Agosto a setiembre |
67 (62,0) |
0,75 (0,63 - 0,90) |
0,75 (0,63 - 0,89) |
|
Azitromicina |
|
|
|
|
Abril a mayo |
67 (84,8) |
Ref+CE23 |
Ref |
|
Junio a julio |
86 (46,0) |
0,54 (0,45 - 0,65) |
0,55 (0,45 - 0,66) |
|
Agosto a setiembre |
21 (19,3) |
0,23 (0,15 - 0,34) |
0,22 (0,15 - 0,33) |
|
Hidroxicloroquina |
|
|
|
|
Abril a mayo |
67 (84,8) |
Ref |
Ref |
|
Junio a julio |
28 (15,1) |
0,18 (0,12 - 0,25) |
0,18 (0,13 - 0,25) |
|
Agosto a setiembre |
0 (0,0) |
No calculable |
No calculable |
|
Ivermectina |
|
|
|
|
Abril a mayo |
27 (34,2) |
Ref |
Ref |
|
Junio a julio |
52 (27,8) |
0,81 (0,55 - 1,19) |
0,84 (0,57 - 1,23) |
|
Agosto a setiembre |
4 (3,7) |
0,11 (0,04 - 0,30) |
0,10 (0,04 - 0,28) |
|
Pulso de corticoides |
|
|
|
|
Abril a mayo |
41 (51,3) |
Ref |
Ref |
|
Junio a julio |
32 (17,1) |
0,33 (0,23 - 0,49) |
0,32 (0,22 - 0,48) |
|
Agosto a setiembre |
8 (7,3) |
0,14 (0,07 - 0,29) |
0,14 (0,07 - 0,28) |
|
Anticoagulación profiláctica |
|
|
|
|
Abril a mayo |
28 (35,9) |
Ref |
Ref |
|
Junio a julio |
24 (12,9) |
0,36 (0,22 - 0,58) |
0,33 (0,20 - 0,55) |
|
Agosto a setiembre |
14 (12,8) |
0,36 (0,20 - 0,63) |
0,35 (0,20 - 0,62) |
|
Tocilizumab |
|
|
|
|
Abril a mayo |
12 (15,4) |
Ref |
Ref |
|
Junio a julio |
20 (10,7) |
0,70 (0,36 - 1,35) |
0,64 (0,33 - 1,25) |
|
Agosto a setiembre |
16 (14,8) |
0,96 (0,48 - 1,92) |
0,88 (0,44 - 1,76) |
a RP ajustado por sexo, edad (en terciles), SatO2/FiO2 (en terciles), y tiempo desde el inicio de síntomas hasta la hospitalización (en terciles).
RP: razones de prevalencia, IC 95%: intervalo de confianza al 95%.
DISCUSIÓN
Se evidenció un aumento en el uso de cuatro fármacos antes de la hospitalización (azitromicina, ivermectina, corticoides y ceftriaxona). Una explicación plausible es la adopción de ivermectina y azitromicina como tratamiento en casos leves ambulatorios de COVID-19 por establecimientos de atención primaria de salud, gobiernos regionales o instituciones públicas. Dicha recomendación fue efectuada por el Ministerio de Salud en abril del 2020 (7), sin evidencia clara de beneficio (6).
Adicionalmente, en el Perú se vio un incremento de infodemia por redes sociales, conferencias, chats o conversaciones cotidianas, compartiendo experiencias supuestamente exitosas de tratamiento contra el COVID-19; lo cual pudo aumentar el uso de diversos fármacos (por indicación del personal de salud o por automedicación), como corticoides y antibióticos de manera extrahospitalaria (10).
Con respecto al uso de fármacos durante la hospitalización, se encontró una disminución de la frecuencia de uso de seis fármacos (ceftriaxona, azitromicina, hidroxicloroquina, ivermectina, pulso de corticoides y anticoagulación profiláctica) y un aumento en el uso de anticoagulación.
Inicialmente, ante la falta de evidencia de calidad, el manejo hospitalario de la COVID-19 en Perú varió de acuerdo con el hospital (11), basándose en los lineamientos establecidos por el MINSA (7,8,9).
En el caso del Hospital Nacional Dos de Mayo, en abril del 2020 se estableció un protocolo de manejo de COVID-19 (12), recomendando el uso de hidroxicloroquina, azitromicina e ivermectina en pacientes hospitalizados; lo cual explicaría el alto uso de dichos tratamientos en los periodos iniciales por nuestro estudio. Sin embargo, dichos medicamentos fueron retirados del protocolo del hospital en julio del 2020, por falta de evidencia clínica (13,14), lo que se relaciona con el posterior descenso en su uso.
Encontramos que siete de cada 10 pacientes hospitalizados recibieron ceftriaxona. Esto puede deberse a que, durante el inicio de la pandemia, se pensó que la COVID-19 podría tener una importante sobreinfección bacteriana (como ha sucedido en otras enfermedades) (3), y a la dificultad para tomar todos los cultivos bacterianos necesarios en el hospital. A pesar de que actualmente se conoce que la frecuencia de sobreinfección bacteriana en pacientes hospitalizados por la COVID-19 es baja (4), otros estudios realizados al inicio de la pandemia también han reportado un alto uso de antibióticos (5,15), e incluso en estudios realizados antes de la pandemia en el mismo Hospital Nacional Dos de Mayo (16). Esto resulta relevante, pues el uso innecesario de antibióticos incrementaría la circulación de microorganismos multirresistentes (17).
En abril del 2020, el MINSA incluyó en sus lineamientos para los casos moderados a severos, el uso de corticosteroides en pulsos (dosis altas) (7). Sin embargo, en junio del 2020 el ensayo Recovery encontró que el tratamiento con dexametasona a una dosis de 6mg/día por un máximo de 10 días podría reducir la mortalidad en pacientes con COVID-19 con apoyo respiratorio (18). Concordantemente, en octubre del 2020 el MINSA adoptó estas dosis de corticoides (9). Dichos cambios pueden explicar la tendencia de uso de corticoides encontrados en este estudio.
Encontramos que, el uso de anticoagulación a dosis profiláctica disminuyó al pasar los meses, en tanto que su uso a dosis plena fue en aumento. El MINSA en abril del 2020 recomendó su uso en dosis profilácticas para casos leves si presentaban factores de riesgo para eventos tromboembólicos, en casos moderados a dosis profilácticas o intermedias y en casos severos anticoagulación plena (19). Asimismo, la Sociedad Americana de Hematología recomendaba utilizarla de acuerdo con el criterio clínico del médico tratante (20).
Algunas potenciales limitaciones del estudio fueron: 1) En la recolección de datos de las historias clínicas se pudieron cometer errores, por lo cual se realizó una validación del llenado, como se explica en la metodología. 2) Algunos confusores importantes como el profesional que atendió al paciente, su estado cognitivo, u otras comorbilidades, no fueron recolectadas. 3) Se consideró usar como variable independiente la fecha de ingreso, a pesar de que la estancia hospitalaria fue variable entre los pacientes, bajo la suposición de que el uso sistemático de fármacos en el hospital se daría desde los primeros días. 4) No se pudo indagar quién indicó los fármacos prehospitalarios ni su posología. Asimismo, al ser esta variable recolectada por autoreporte, está sujeta a sesgos de memoria y de deseabilidad social. 5) Algunos intervalos de confianza son amplios debido al limitado tamaño de muestra. A pesar de sus limitaciones, este es a nuestro entender el primer estudio en Perú acerca de la tendencia del uso de fármacos en el contexto de la pandemia por la COVID-19, tomando en cuenta una muestra representativa de uno de los principales hospitales de Lima.
En conclusión, este estudio muestra cómo se han ido modificando las tendencias del uso de fármacos prehospitalarios y hospitalarios para la COVID-19, durante la primera ola, en un hospital peruano. Encontramos un aumento en el uso de cuatro fármacos antes de la hospitalización (azitromicina, ivermectina, corticoides y ceftriaxona), así como una disminución de la frecuencia de otros (ceftriaxona, azitromicina, hidroxicloroquina, ivermectina, pulso de corticoides, y anticoagulación profiláctica) y el aumento en el uso de anticoagulación plena durante la hospitalización.
Contribuciones de los autores: NEC, DRG y ATR contribuyeron a la concepción y diseño del artículo. NEC, MTR y DRG realizaron la recolección de datos. NEC, PRG, MTR y ATR analizaron e interpretaron los datos. FGR, MTR, DRG, NEC Y ATR realizaron la redacción del estudio. PRG y ATR fueron los asesores estadísticos. DRG, MTR y NEC fueron asesores técnicos.
Conflictos de interés: DRG, NEC, PRG y MTR laboraron en el Hospital Nacional Dos de Mayo durante el periodo evaluado. Los demás autores declaran no tener conflictos de interés con respecto al presente estudio.
Financiamiento: el estudio fue autofinanciado por los investigadores.
REFERENCIAS BIBLIOGRÁFICAS
1. Tuccori M, Convertino I, Ferraro S, Cappello E, Valdiserra G, Focosi D, et al. The Impact of the COVID-19 "Infodemic" on Drug-Utilization Behaviors: Implications for Pharmacovigilance. Drug Saf. 2020;43(8):699–709. doi: 10.1007/s40264-020-00965-w.
2. Bajwah S, Wilcock A, Towers R, Costantini M, Bausewein C, Simon ST, et al. Managing the supportive care needs of those affected by COVID-19. Eur Respir J. 2020;55(4). doi: 10.1183/13993003.00815-2020.
3. Langford BJ, So M, Raybardhan S, Leung V, Westwood D, MacFadden DR, et al. Bacterial co-infection and secondary infection in patients with COVID-19: a living rapid review and meta-analysis. Clin Microbiol Infect. 2020;26(12):1622–9. doi: 10.1016/j.cmi.2020.07.016.
4. Lansbury L, Lim B, Baskaran V, Lim WS. Co-infections in people with COVID-19: a systematic review and meta-analysis. J Infect. 2020;81(2):266–75. doi: 10.1016/j.jinf.2020.05.046.
5. Chedid M, Waked R, Haddad E, Chetata N, Saliba G, Choucair J. Antibiotics in treatment of COVID-19 complications: a review of frequency, indications, and efficacy. J Infect Public Health. 2021;14(5):570–6. doi: 10.1016/j.jiph.2021.02.001.
6. Bhimraj A, Morgan RL, Shumaker AH, Lavergne V, Baden L, Cheng VC-C, et al. Infectious Diseases Society of America Guidelines on the Treatment and Management of Patients with COVID-19. Clin Infect Dis. 2020;ciaa478. doi: 10.1093/cid/ciaa478.
7. Ministerio de Salud. Resolución Ministerial N° 193-2020-MINSA [Internet]. Lima: Dirección General de Intervenciones Estratégicas en Salud Pública. MINSA; 2020 [citado 20 de mayo de 2021]. Disponible en: https://www.gob.pe/institucion/minsa/normas-legales/473575-193-2020-minsa.
8. Ministerio de Salud. Resolución Ministerial N° 270-2020-MINSA [Internet]. Lima: Dirección General de Intervenciones Estratégicas en Salud Pública. MINSA; 2020 [citado 7 de mayo de 2021]. Disponible en: https://www.gob.pe/institucion/minsa/normas-legales/563764-270-2020-minsa.
9. Ministerio de Salud. Resolución Ministerial N° 839-2020-MINSA [Internet]. Lima: Dirección General de Intervenciones Estratégicas en Salud Pública. MINSA; 2020 [citado 7 de mayo de 2021]. Disponible en: https://www.gob.pe/institucion/minsa/normas-legales/1264399-839-2020-minsa.
10. Martinez‐Rivera RN, Taype‐Rondan A. Overmedication in COVID-19 Context: A Report From Peru. J Clin Pharmacol. 2020;60(9):1155–6. doi: 10.1002/jcph.1704.
11. Instituto de Evaluación de Tecnologías en Salud e Investigación. Farmacovigilancia intensiva al tratamiento farmacológico de COVID-19 en pacientes moderados y graves [Internet]. Informe de Farmacovigilancia N° 06- CRIFyT-IETSI 2020 [Citado 15 de noviembre 2020]. Disponible en: http://www.essalud.gob.pe/ietsi/pdfs/farmacoytecno/covid_19/INFORME_FINAL_FV_INTENSIVA.pdf.
12. Comité Técnico Asesor COVID-19 del Hospital Nacional Dos de Mayo. Resolución Directoral N° 050-2020-Hospital Nacional Dos de Mayo [Internet]. [citado 21 de octubre de 2021]. Disponible en: http://hdosdemayo.gob.pe/portal/resoluciones-directorales-2020/.
13. Instituto de Evaluación de Tecnologías en Salud e Investigación. Guía de Práctica Clínica para el Manejo de COVID-19: Guía en Versión Extensa. Versión 1, mayo 2021. Lima: EsSalud; 2021. Disponible: http://www.essalud.gob.pe/ietsi/pdfs/guias/GPC_COVID_19_Version_corta.pdf.
14. Instituto de Evaluación de Tecnologías en Salud e Investigación. Guía de Práctica Clínica para el Manejo de COVID-19: Guía en Versión Extensa. Versión 2, julio 2021. Lima: EsSalud; 2021.Disponible: http://www.essalud.gob.pe/ietsi/pdfs/guias/GPC_COVID_19_Vers_cortaV2_Julio2021.pdf.
15. Huttner BD, Catho G, Pano-Pardo JR, Pulcini C, Schouten J. COVID-19: don't neglect antimicrobial stewardship principles!. Clin Microbiol Infect. 2020;26(7):808-810. doi: 10.1016/j.cmi.2020.04.024.
16. Resurrección-Delgado C, Chiappe-Gonzalez A, Bolarte-Espinoza J, Martínez-Dionisio L, Muñante-Meneses R, Vicente-Lozano Y, et al. Uso de antibióticos en pacientes internados en un hospital nacional de Lima, Perú. Rev Peru Med Exp Salud Publica. 2020;37(4):620-6. doi: 10.17843/rpmesp.2020.374.5073.
17. Rawson TM, Moore LSP, Castro-Sanchez E, Charani E, Davies F, Satta G, et al. COVID-19 and the potential long-term impact on antimicrobial resistance. J Antimicrob Chemother. 2020;75(7):1681–4. doi: 10.1093/jac/dkaa194.
18. RECOVERY Collaborative Group, Horby P, Lim WS, Emberson JR, Mafham M, Bell JL, et al. Dexamethasone in Hospitalized Patients with Covid-19. N Engl J Med. 2021;384(8):693-704. doi: 10.1056/NEJMoa2021436.
19. Ministerio de Salud. Resolución Ministerial N° 240-2020-MINSA [Internet]. Lima: Dirección General de Intervenciones Estratégicas en Salud Pública [citado 7 de mayo de 2021]. Disponible en: https://www.gob.pe/institucion/minsa/normas-legales/542922-240-2020-minsa.
20. COVID-19 and VTE/Anticoagulation: Frequently Asked Questions [Internet]. [citado 7 de mayo de 2021]. American Society of Hematology. Disponible en: https://www.hematology.org:443/covid-19/covid-19-and-vte-anticoagulation.
Citar como: Echevarria Castro N, Rojo García D, Torpoco Rivera M, Rondán-Guerrero P, García-Rojas F, Taype-Rondan A. Tendencias en el uso de fármacos para la COVID-19 durante la primera ola de la pandemia en un hospital de Lima, Perú. Rev Peru Med Exp Salud Publica. 2021;38(4):610-6. doi: https://doi.org/10.17843/rpmesp.2021.384.8820.
Correspondencia: Nataly Elda Echevarria Castro; natalyechevarria1104@gmail.com
Recibido: 03/07/2021
Aprobado: 03/11/2021
En Línea: 22/12/2021